97
Glykogen – Glykoside
Anmerkung: Fortsetzung des Artikels 'Glykocholsäure'
sehr schwer löslich ist, so übt sie im freien Zustande kaum die Wirkung einer Säure aus, und es wird daher im tierischen
Organismus der aus dem Magen kommende stark saure Speisebrei im Dünndarm durch die dort mit ihm
zusammentreffende Galle neutralisiert.
Glykogen, Leberstärke, eine der Stärke und dem
Dextrin nahestehende Verbindung von der Zusammensetzung
(C6H10O5)x, deren
Molekulargröße unbekannt ist. Das G. wird im Tierkörper erzeugt, findet sich in den Muskeln und wird in reichlichster
Menge während des Verdauungsprozesses in der Leber aufgespeichert. Zur Darstellung wird die zerhackte Leber eines
frisch geschlachteten Tieres mit Wasser ausgekocht und die von Eiweißstoffen u.s.w. befreite und filtrierte Lösung mit
Alkohol gefällt. Es ist ein mehlartiges, in Alkohol und Äther unlösliches weißes Pulver. In Wasser löst es sich leicht, jedoch
nur zu einer kleisterartig opalisierenden Flüssigkeit, welche die Polarisationsebene des Lichts nach rechts dreht. Durch
tierische Fermente, Speichel, Pankreas, Lebergewebe,wird es leicht gespalten, zunächst in ein dextrinähnliches
Kohlehydrat und einen maltoseartigcn Zucker. Bei weiterer Spaltung und beim Kochen mit verdünnten Säuren liefert es
Traubenzucker. Im Organismus entsteht das G. aus den Kohlehydraten und dem Eiweiß der Nahrung. Es dient dem
Körper als Kraft- und Wärmequelle, wird bei der Verdauung im Überschuß in der Leber aufgespeichert, um bei später
eintretendem Mangel dem Blute allmählich wieder zuzufließen, indem es wahrscheinlich vorher in Traubenzucker zerfällt.
Bei längerm Hungern verschwindet das G. aus der Leber und den Muskeln.
Glykokóll (Glycocoll,
Glykochol), Glycin,
Leimsüß, Leimzucker, eine Verbindung von
der Zusammensetzung C2H5O2N, die beim
Kochen von Leim, Hippursäure und Glykocholsäure mit verdünnten Säuren als Spaltungsprodukt auftritt. Es ist die
einfachste Amidosäure (s. d.), Amidoessigsäure,
NH2•CH2•COOH. Das G. ist auch synthetisch auf
verschiedenen Wegen gewonnen worden, wird aber am besten aus der Hippursäure (Benzoylglykokoll) dargestellt, indem
man dieselbe mit Salzsäure kocht, die auskrystallisierte Benzoesäure abfiltriert und aus der eingedampften Lösung das
salzsaure Salz des G. krystallinisch gewinnt. Das G. bildet farblose große rhombische Krystalle, löst sich in Wasser leicht,
in Alkohol und Äther sehr schwer, schmeckt süß, schmilzt bei 236° und zersetzt sich bei stärkerm Erhitzen. Wie alle
Amidosäuren vereinigt das G. in sich die Eigenschaften einer Ammoniakbase und einer Säure; die Lösung reagiert daher
neutral, und es giebt sowohl mit Säuren als auch mit Basen Salze, die gut krystallisieren. Das salzsaure Salz hat die Formel
HCl•NH2•CH2•COOH. Besonders charakteristisch ist das
Kupfersalz (Glykokollkupfer),
(C2H4NO2)2Cu+H2O,
das aus der heißen Lösung von Kupferoxyd in G. in dunkelblauen Nadeln krystallisiert. Das G. liefert einen Äthylester,
NH2•CH2•COOC2H5, der durch
Behandlung mit salpetriger Säure in den interessanten Ester der Diazoessigsäure übergeht.
Sarkosin und Betain sind Abkömmlinge des
G., die Methylgruppen am Stickstoff enthalten.
Glykol, Äthylenglykol, der einfachste der zweiwertigen
Alkohole oder Glykole (s. d.). Es ist eine bei 197" siedende Flüssigkeit von der Zusammensetzung
CH2OH•CH2OH, die aus Äthylenbromid
↔ und Kaliumcarbonat gewonnen wird. Oxydationsmittel führen G. in Glykolsäure und Oxalsäure über.
Glykole, Bezeichnung für die zweiwertigen Alkohole (s. d.). Die G.
enthalten also zwei Hydroxylgruppen, (OH)2. Sie sind neutrale dicke
Flüssigkeiten, schmecken süßlich und stehen in ihren Eigenschaften zwischen den einwertigen Alkoholen und dem
dreiwertigen Glycerin. Sie sind im Wasser sehr leicht, in Äther weniger löslich und sieden bei viel höhern Temperaturen als
die einwertigen Alkohole. Das einfachste Glykol, das Glykol (s.d.) schlechthin, ist das Äthylenglykol.
Glykolsäure, eine organische Säure, die sich aus Glykol (s. d.) durch
Oxydation bildet und sich in natürlichem Zustande in den unreifen Weintrauben, den Blättern des wilden Weins u. s. w.
findet. Sie hat die Formel CH2OH•COOH und läßt sich danach auch
als Oxyessigsäure betrachten. Man gewinnt sie am besten durch Kochen einer
wässerigen Lösung von Chloressigsäure mit kohlensaurem Kalk. Sie krystallisiert in Nadeln, die bei 80° schmelzen, und
zeigt sowohl die Reaktionen einer Säure wie die eines Alkohols. Als Säure giebt sie mit Metallen Salze, mit Alkoholen
Ester, z. B. den Äthylester,
CH2OH•COOC2H5, ferner Amid und Chlorid,
alle wegen der vorhandenen Hydroxylgruppe mit Alkoholcharakter. Umgekehrt giebt die G. als Alkohol mit andern Alkoholen
Äther, z. B. Äthylglykolsäure,
C2H5•O•CH2•COOH, mit Säuren Ester,
z. B. Acetylglykolsäure, CH3•CO•O•COOH, Amine, wie das
Glykokoll (s.d.), welche Verbindungen dann noch die Reaktionen einer Säure zeigen.
Glykolylharnstoff, Glykolursäure, s. Hydantoin.
Glykoneischer Vers, Glykonischer Vers oder
Glyconeus, ist eine nach dem griech. Dichter Glykon benannte Verszeile von der
Form
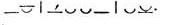
Textfigur:
S. Asklepiades.
Glykose oder Glukose, Bezeichnung einerseits für
Traubenzucker (s. d.), andererseits für alle Zuckerarten von der Zusammensetzung
C6H12O6, die zu der Gruppe des
Traubenzuckers gehören, also Lävulose (s. Fruchtzucker), Mannose (s. d.),
Galaktose (s. d.), Acrose (s. d.). Sie krystallisieren meist, sind in Wasser sehr
leicht, in absolutem Alkohol schwer, in Äther nicht löslich. Ihrer chem. Konstitution nach sind sie Keton- oder
Aldehydalkohole: sie reduzieren alkalische Kupferlösungen (Fehlingsche Lösung), vergären leicht durch Hefe u. s. w.
Sie entstehen meist durch Spaltung unter Wasseraufnahme aus den Kohlehydraten der Rohrzucker- und Stärkegruppe.
Es kann dies sowohl durch die Wirkung von Fermenten, als auch von verdünnten Säuren in der Wärme bewirkt werden.
Auch durch Oxydation sechswertiger Alkohole, wie des Mannits (s.d.), und in
neuester Zeit durch Synthese sind G. erhalten worden.
Glykoside oder Glukoside, organische Pflanzenstoffe,
die durch Fermente oder durch Alkalien oder Säuren unter Aufnahme von Wasser derartig gespalten werden, daß als eins
der Spaltungsprodukte eine Zuckerart, meist Traubenzucker, gebildet wird. Sie sind also ätherartige Verbindungen der
Zuckerarten. Als Beispiel diene das Amygdalin (s. d.), das durch das Emulsin
(s. d.) oder beim Erwärmen mit verdünnten Säuren in Traubenzucker, Bittermandelöl und Blausäure gespalten wird:
Anmerkung: Fortgesetzt auf Seite 98.
